CMDCAS產品注冊
- 立即咨詢
-
全國服務熱線:
400-888-7587

400-888-7587
? 辦理介紹 / Introduction
? 加拿大醫療器械法規將醫療器械分為I, II,III,IV四個分類,依次依據風險大小,如I類器械為最低風險,IV類器械風險為最高。為此針對制造者提出的產品注冊要求也是逐級增加,要求制造者實行的體系是愈加詳盡。如I類醫療器械豁免注冊。II,III,IV類器械的注冊要求如下:
1、通用注冊資料:
2、器械的名稱;
3、器械的分類;
4、器械的標識;
5、產品標簽上出現的制造者名稱、地址;
6、若制造地點與d)不同,則制造地名稱、地址;
? II 類器械注冊附加資料:
? 所制造、銷售或代理的器械關于醫用條件的目的及用途的描述;
? 為滿足安全和有效性要求所符合的標準的清單;
? 由制造者的高層主管作的安全有效性符合聲明;
? 由制造者的高層主管作的器械標簽符合加拿大醫療器械法規的聲明;
? 若是近病人體外診斷設備(即不在醫院而是在例如家庭使用的設備),制造者的高層主管應聲明已用代表預期使用者的人體物質在與預期使用條件類似的條件下進行了研究性測試;
? 由CMDCAS認可機構頒發的CAN/CSA-ISO 13485體系證書。
? III類器械注冊的附加條件:
? 器械及在其制造及包裝中所用材料的描敘;
? 所制造、銷售和代理的器械在其允許的醫療條件、目的和用途下的性能描述;
? 除加拿大外的器械獲準銷售的國家清單、售出數量,以及報導的問題及召回情況;
? 器械的設計和制造為滿足安全有效性而采用的標準清單;
? 如果是以無菌出售的器械,則無菌方法描述;
? 制造者為安全有效而進行的研究描述,以及由此得出的結論;
? 器械標簽/復印件;
? 如果為近病人體外診斷設備,用代表目的預期用戶的人體物質,以在使用條件類似的條件下的研究測試的情況;
? 所有與使用、安全和有效有關的公開發布的報告的文獻引用;
? 由加拿大醫療器械【信息咨詢】機構認可的機構所頒發的CAN/CSA-ISO 13485證書。
? IV類醫療器械的附加材料為:
? 器械及制造和包裝過程中所有材料的描述;
? 所制造、銷售或代理的器械所允許的醫療條件、目的和用途的器械特性描敘;
? 除加拿大以外器械獲準銷售的國家,售出數量,以及報告器械的問題及召回情況;
? 風險評估情況包括風險分析、風險評價,以及評價風險滿足安全有效的糾正措施;
? 與器械相關的質量計劃,如特定的質量實踐,資源及行動的程序;
? 制造和包裝中使用的材料的參數;
? 器械的制造過程;
? 設計、制造中為滿足安全有效要求而采用的標準清單;
? 制造者為證明滿足安全有效要求而進行的所有研究的詳細情況,包括:i) 臨床前研究和臨床研究; ii) 過程驗證研究; iii) 適用時,軟件驗證研究,和 iv)文獻研究;
? 若非體外診斷設備、取自動物組織或組織衍生產物的器械,其客觀生物安全證據;
? 若為近病人體外診斷設備,針對代表預期用戶的人體物質且在相似使用條件下進行的研究測試的詳細情況;
? 制造者依據(i)款研究得出的結論;
? 制造者依據(h)款研究的總述及由此得出的結論;
? 與器械的使用、安全和有效相關的公開發布報道的文獻;
? 器械標簽的復印件;
? 由加拿大醫療器械機構認可的機構所頒發的CAN/CSA-ISO 13485證書。
醫療器械許可證發布后,每年11月1日應由制造者向加拿大衛生部提出再確認。取消生產許可證應在停止加拿大銷售的30日之內提出。
? 辦理流程 / Processing process
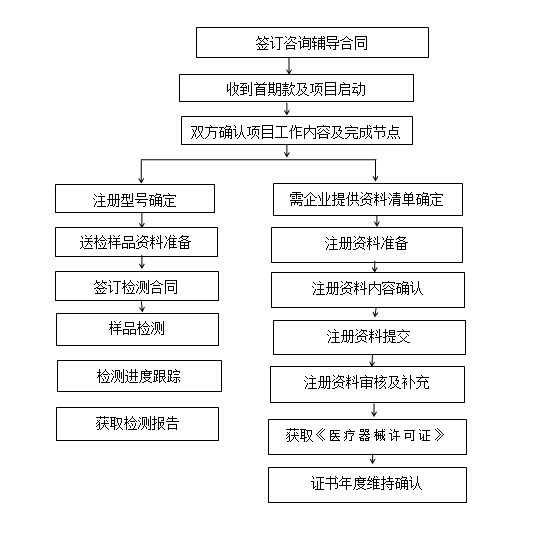
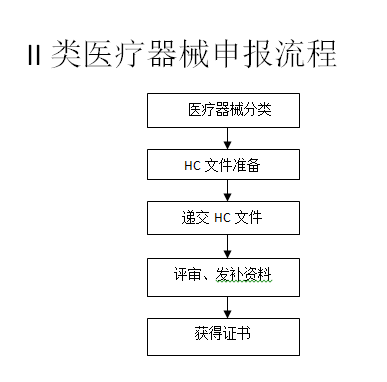
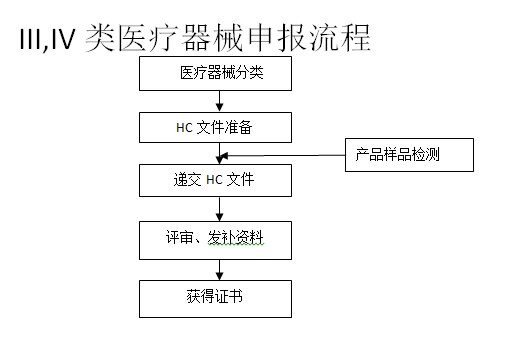
? 行政時間 / Administration Service Time
業務名稱 | 官方時間 |
II類HC | 90 |
III,IV類HC | 90 |
? 金飛鷹相關服務 / Golden Eagle related services
● 代表性樣檢驗樣品確認
● 樣品檢驗機構確認
● 檢驗標準確定
● 相關資料合規性審核
● 注冊資料編制
● 注冊資料提交
● 證書年度維持確認
● 其它必要的工作
全面解決您的研發、生產、驗收、營銷全流程問題

practical experience
2000多個二、三類醫械項目經驗沉淀,為你分配做過相同案例的實戰老師。
Professional translation
匯聚7大語種專業翻譯精英,多年醫械行業翻譯經驗,能準確翻譯專業名詞及用語。
Software development
強大的軟件研發團隊,已為集團研發出成熟的項目管理軟件,可提供軟件定制服務。
Group supply chain
嚴選數十個優秀的醫械行業服務機構,可為客戶推薦更實惠的醫械配套服務。
多次創造二三類高風險產品一次性通過的行業紀錄
項目狀態:已結案
項目輔導老師:李老師
項目狀態:已結案
項目輔導老師:車老師
項目狀態:已結案
項目輔導老師:王老師
項目狀態:已結案
項目輔導老師:黃老師