文章出處:行業干貨 網責任編輯: 金飛鷹 閱讀量: 發表時間:2025-08-05
國家藥監局發布的《關于進一步加強醫療器械注冊人委托生產監督管理的公告(2024年第38號)》提到:“受托生產企業應當建立生產放行規程,明確生產放行的標準、條件,對醫療器械生產過程進行審核,對產品進行檢驗,確認符合標準、條件的,方可生產放行。”
那么生產放行必須把產品技術要求作為放行標準嗎?是否可以根據產品特點設定生產放行標準,不把產品技術要求當成產品放行標準呢?
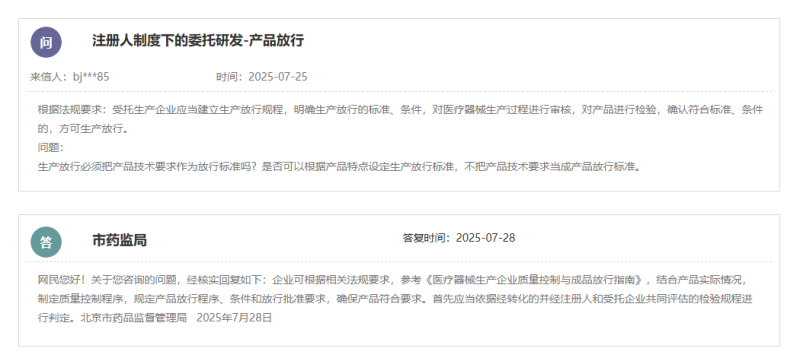
根據北京市藥監局的答復,企業可根據相關法規要求,參考《醫療器械生產企業質量控制與成品放行指南》,結合產品實際情況,制定質量控制程序,規定產品放行程序、條件和放行批準要求,確保產品符合要求。首先應當依據經轉化的并經注冊人和受托企業共同評估的檢驗規程進行判定。
醫療器械注冊咨詢認準金飛鷹
深圳:0755-86194173
廣州:020 - 82177679
四川:028 - 68214295
湖南:0731-22881823
湖北:181-3873-5940
江蘇:135-5494-7827
廣西:188-2288-8311
海南:135-3810-3052
重慶:135-0283-7139