文章出處:行業干貨 網責任編輯: 金飛鷹 閱讀量: 發表時間:2024-02-29
《醫療器械監督管理條例》第二十五條指出:“進行醫療器械臨床評價,可以根據產品特征、臨床風險、已有臨床數據等情形,通過開展臨床試驗,或者通過對同品種醫療器械臨床文獻資料、臨床數據進行分析評價,證明醫療器械安全、有效。”
那么,醫療器械注冊申請人到底要如何選擇合適的臨床評價路徑呢?
注冊申請人可參照《決策是否開展醫療器械臨床試驗技術指導原則》判定是否需要開展臨床試驗,并結合國家藥監局器審中心去年發布的《醫療器械分類目錄》子目錄相關產品臨床評價推薦路徑的通告,選擇適宜的臨床評價路徑。
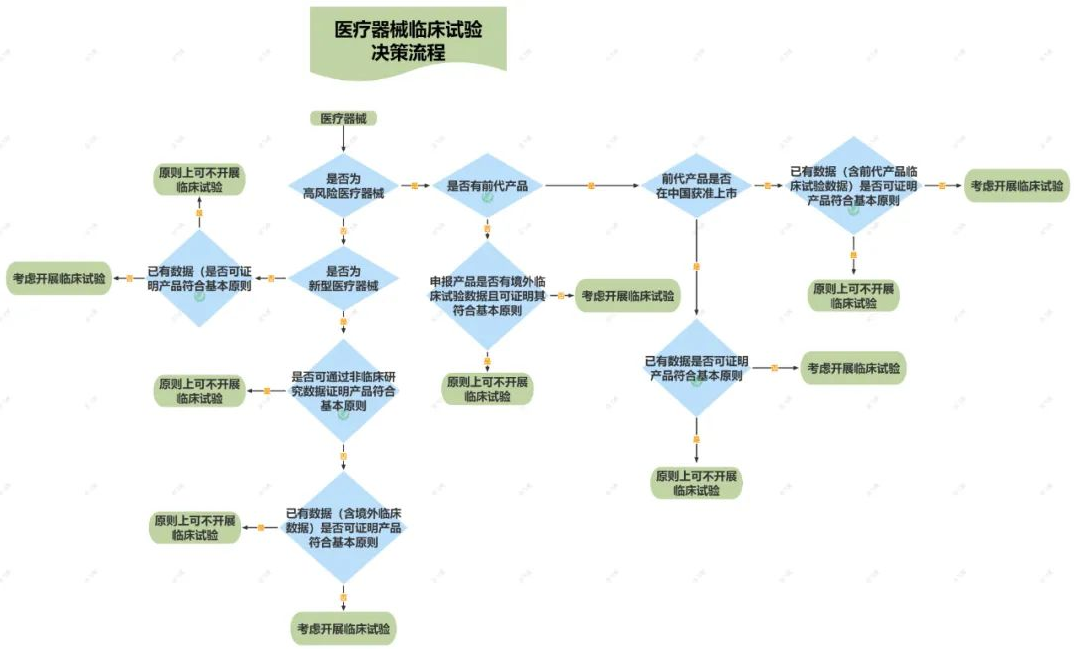
? 醫療器械臨床試驗決策流程圖
醫療器械注冊咨詢認準金飛鷹 深圳:0755-86194173 廣州:020 - 82177679 湖南:0731-22881823 四川:028 - 68214295